Гиполипидемические средства. Характеристика
В зависимости от соотношения основных компонентов выделяют 4 класса липопротеидов. Наиболее крупные частицы – хиломикроны – являются основной транспортной формой экзогенного жира и состоят на 85% из триглицеридов. Стабилизируют оболочку хиломикронов белок и фосфолипиды.
В печени триглицериды, холестерин и фосфолипиды включаются в состав других белково-липидных комплексов: пре-бета-липопротеидов (липопротеидов очень низкой плотности – ЛПОНП) и бета-липопротеидов (липопротеидов низкой плотности – ЛПНП), которые циркулируют в крови и обладают агрессивными атерогенными свойствами. Клетки человека нуждаются в холестерине, который переносится из плазмы к клетке с помощью липопротеидов низкой плотности (ЛПНП). Проникнуть внутрь клетки холестерин может, лишь взаимодействуя с ЛПНП-рецепторами, располагающимися на поверхности и способными доставить холестерин внутрь клетки. Основным органом, удаляющим холестерин и липопротеиды низкой плотности из плазмы, является печень, поэтому чем больше число ЛПНП-рецепторов, тем ниже уровень атерогенного холестерина в плазме.
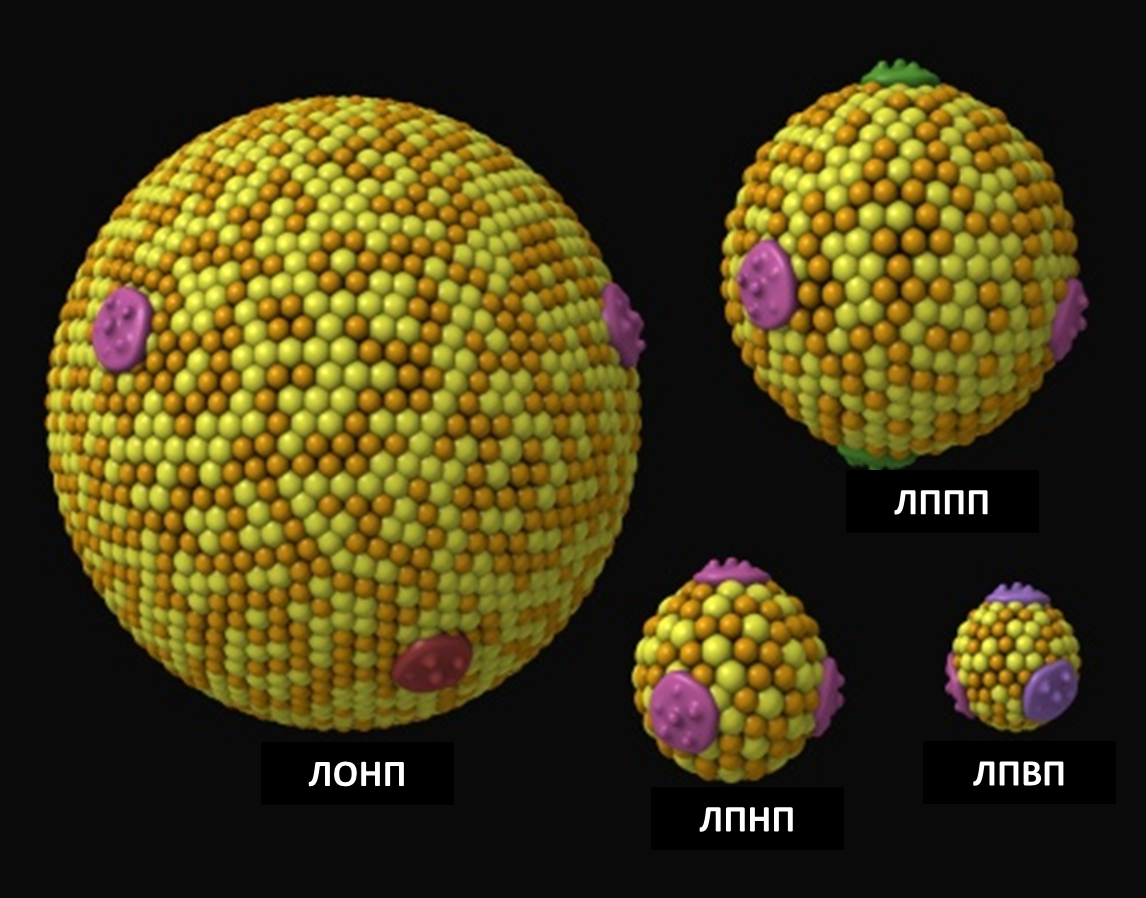
ЛПОНП состоят преимущественно из эндогенных триглицеридов (55%) и небольшого количества холестерина. ЛПНП соответствуют бета-липопротеидам. Они содержат большое количество холестерина и его эфиров (до 45%) и являются главными транспортными носителями этого стерина. Помимо холестерина, они содержат триглицериды – 10% и фосфолипиды – 20%. Вследствие наличия в ЛПНП апопротеина В к этим частицам легко образуются антитела, синтезируемые в печени.
Значительно меньше липидов находят в альфа-липопротеидах (липопротеиды высокой плотности), которые содержат около 50% белка и фосфолипидов и обладают свойствами удалять холестерин с адвентиции сосудов и других тканей и транспортировать в печень для катаболизма.
Выделяют также так называемые флотирующие липопротеиды. Этот промежуточный класс липопротеидов содержит очень большое количество холестерина; они образуются в процессе превращения ЛПОНП в ЛПНП и имеют значение в развитии атеросклероза.
Важнейшим мероприятием в плане профилактики атеросклероза и выявления нарушений липидного обмена, а также разработки мероприятий по борьбе с этими патологическими факторами является определение холестерина в плазме крови.
Диагностика дислипопротеидемий и методы лечения. Уровень холестерина (ХС) сыворотки определяют для того, чтобы выявить больных с выраженными нарушениями липидного обмена и выделить группы риска.
Нормальный уровень общего ХС крови менее 200 мг%. В некоторых странах верхняя граница нормы иная. Лица, относящиеся к данной группе, должны быть ознакомлены с общими принципами диеты, информированы о существовании факторов риска ИБС и возможности влиять на них. Уровень общего ХС следует определить повторно через 5 лет, поскольку со временем он может измениться. При пограничном уровне ХС (200-240 мг%) тактика лечения определяется наличием или отсутствием факторов риска. При их отсутствии назначают диету и ежегодно следят за уровнем холестерина и выявляют факторы риска. При наличии двух и более факторов риска тщательно определяют профиль липопротеидов.
При уровне холестерина выше 240 мг% анализируют профиль липопротеидов и назначают диетическое лечение.
При нормальном уровне холестерина ЛПНП (менее 130%) рекомендуют соблюдать диету и проводят беседу о вреде факторов риска. Лицам с пограничным уровнем ХС ЛПНП, отсутствием ИБС и двух факторов риска рекомендуют диету и контроль за уровнем ХС один раз в год. При наличии ИБС или двух факторов риска, так же как у лиц с высоким уровнем ХС ЛПНП, проводят тщательное клинико-лабораторное исследование для выявления вторичных гиперлипопротеидемий и наследственных нарушений обмена.
При гипертриглицеридемии мероприятия начинают с диеты.
Причины вторичной гиперлипидемии – нарушения питания, гипотиреоз, сахарный диабет, нефротический синдром, уремия и диспротеинемия. На содержание липидов могут влиять и некоторые лекарственные средства. Так, на уровень общего ХС, ТГ и ХС ЛПНП влияют тиазидные диуретики, адреноблокаторы (особенно неселективные), глюкокортикоиды, эстрогены, прогестины, ретиноиды, анаболические гормоны и алкоголь.
Семейные гиперлипопротеинемии характеризуются чрезвычайно высоким содержанием липидов в сыворотке и требуют, кроме соблюдения диеты, медикаментозного лечения.
Лечение начинают с диетотерапии. В дальнейшем может возникнуть необходимость в медикаментозном лечении, которое не исключает соблюдения диеты.
Первичные гиперлипидемии. Семейная гиперхолестеринемия (СГХС) – аутосомно-доминантное заболевание, обусловленное отсутствием рецепторов к ЛПНП. Диагностируется в 0,5% популяции. При гетерозиготной СГХС число рецепторов к ЛПНП составляет 50% от нормы, а уровень ХС ЛПНП повышен; содержание общего ХС – 350-550 мг%. Лечение, помимо диетотерапии, обязательно включает прием гиполипидемических препаратов.
При гомозиготной СГХС число рецепторов к ЛПНП крайне мало или они вообще отсутствуют, резко повышен уровень ХС ЛПНП. Содержание общего ХС – до 1000 мг%. Это заболевание встречается крайне редко, многие больные не доживают до 30 лет. Диета и медикаментозное лечение малоэффективны, слабо помогают плазмаферез и трансплантация печени.
При смешанной семейной гиперлипопротеидемий, при которой довольно часто обнаруживается дефицит липопротеидлипазы, лечение начинают с диеты, физических упражнений, снижения массы тела и реже прибегают к применению лекарств. Так называемую полигенную гиперхолестеринемию обнаруживают у каждого 10-го больного с содержанием холестерина выше 300 мг%. У этих больных моногенного наследования нет. Эффективно сочетание диетотерапии и медикаментозного лечения.
Гипертриглицеридемия – чаще вторичное проявление ожирения, эндокринных заболеваний, алкоголизма, приема оральных контрацептивов, ретиноидов, бета-адреноблокаторов. Лишь когда уровень триглицеридов выше 500 мг%, можно думать о семейном нарушении липидного обмена.
Дисбеталипопротеидемия (III тип по Fredrickson) – заболевание, обусловленное дефицитом апопротеина Е, находящегося на поверхности ЛПОНП, ответственного за распознавание и захват впоследствии разрушающихся ремнантных частиц рецепторами клеточной поверхности. Биохимически это проявляется повышением уровня триглицеридов и холестерина, накоплением атерогенных ЛПОНП. Дислипидемии ассоциируются с частыми сердечно-сосудистыми заболеваниями.
Гиперхиломикронемия обусловлена отсутствием или дефицитом липопротеидлипазы и ее кофактора и проявляется наличием слоя хиломикронов после центрифугирования плазмы или при электрофорезе, повышением уровня ЛПОНП и хиломикронов.
Снижение уровня ХС ЛПВП менее 35 мг% зависит от двух причин: генетически обусловленной гипо-альфа-липопротеидемии или ятрогенных факторов (курение, ожирение).

Диета. Начало лечения гиперлипопротеидемий предполагает попытку коррекции нарушений липидного метаболизма с помощью диетических мероприятий – снижения уровня холестерина в плазме крови до 130-160 мг% у лиц с пограничным уровнем холестерина с наличием ИБС и факторов риска или их отсутствием.
Диетотерапию проводят в несколько этапов. На первом этапе на долю потребляемых жиров должна приходиться треть калорий, получаемых в течение суток. При этом доля насыщенных жиров не должна превышать 10%, а потребление холестерина – не более 300 мг/сут. Это достигается снижением употребления говядины, свинины, птицы (с птицы обязательно удаляют кожу) и рыбы до 85 г и ограничением мясных блюд до 170 г/сут. Мясные продукты должны быть нежирными, в вареном виде. Исключают пальмовое и кокосовое, сливочное масло, сыры с большим содержанием жиров и цельномолочные продукты. Взамен рекомендуют мягкий маргарин, жидкие растительные масла, сыры и другие молочные продукты низкой жирности. В рекомендуемой диете полиненасыщенные жиры (маргарин, растительные масла) не должны превышать 10% общей калорийности. Избыток полиненасыщенных жирных кислот снижает ХС ЛПВП. Мононенасыщенные жиры должны составлять не более 10-15% общей калорийности пищи. Они содержатся в оливковом масле и некоторых мясных продуктах. Следует ограничить прием таких холестеринсодержащих продуктов, как печень, почки, мозг, поджелудочная железа; за неделю можно съесть не более 4 желтков. На долю углеводов, особенно сложных, должно приходиться 55-60% калорийности; они содержатся в свежих овощах, фруктах и продуктах из цельного зерна.
Через 3 мес при отсутствии снижения уровня холестерина диета должна быть более строгой. Снижают потребление насыщенных жиров до 7% общей калорийности, а холестерина – до 200 мг/сут. Полностью исключают яйца, субпродукты, твердые жиры, сливочное масло, плавленые сыры, животные жиры, шоколад.
При соблюдении диетических мероприятий холестерин в плазме крови можно снизить на 7%; этому способствуют и физические упражнения.
ИНГИБИТОРЫ ГМГ-КОА-РЕДУКТАЗЫ (СТАТИНЫ). В 1976 г. был открыт новый класс антибиотиков – монокалины, которые специфически подавляют активность фермента З-гидрокси-3-метилглютарил коэнзим А (ГМГ-КоА)-редуктазы, катализирующего раннюю реакцию биосинтеза ХС.
Ловастатин (мевакор) представляет собой химическую модификацию продукта, образующегося в процессе ферментации грибкового микроорганизма Aspergillus terreus. С 1987 г. препарат используется более чем в 50 странах мира.
Основная часть ХС, транспортируемая ЛП плазмы, поступает не из внешних источников, а синтезируется в организме, главным образом в печени. Блокируя синтез ХС, мевакор снижает содержание ХС в клетках печени, вследствие чего увеличивается захват липопротеидов гепатоцитами из плазмы крови. Лечение мевакором ведет к значительному снижению уровня общего ХС и ХС ЛПНП – на 20-45% в зависимости от чувствительности больных и суточной дозы. При этом наблюдается также значительное снижение содержания аполипопротеинов В и Е в плазме (на 15-25%). Отмечаются падение уровня ХС ЛПОНП, триглицеридов плазмы (на 10-20%) и повышение ЛПВП (на 6-15%). Такой важный показатель атерогенности плазмы крови, как отношение ХС ЛПНП/ХС ЛПВП, снижается почти на 50%. Выраженный терапевтический эффект в виде снижения ХС ЛПНП (<20%) можно получить у 90% больных с ГЛП IIа типа. Мевакор помогает больным, безуспешно лечащимся холестирамином, колестиполом, никотиновой кислотой, пробуколом. Общее содержание ХС плазмы крови возвращается к исходному уровню через 1 мес после отмены максимальной дозы мевакора – 80 мг. Терапевтический эффект мевакора довольно стабилен, явлений тахифилаксии при длительном лечении не наблюдается.
Препарат быстро всасывается в ЖКТ, особенно при приеме пищи. В плазме крови на 95% связан с белками, в печени подвергается метаболизму с образованием активных метаболитов. Выделяется на 90% с фекалиями и на 10% с мочой. Т1/2 равен 3 ч.
Ловастатин высокоэффективен у больных с наследственной гетерозиготной формой гиперхолестеринемии и у больных с ненаследственной (полигенной) формой первичной гиперхолестеринемии. При гомозиготной семейной гиперхолестеринемии статины не показаны, так как у этих больных отсутствуют ЛПНП-рецепторы в клетках печени, осуществляющие клиренс ЛПНП в ответ на снижение эндогенного пула ХС. Хорошие результаты получены при коррекции вторичной ГЛП у больных с сахарным диабетом и нефротическим синдромом.
Мевакор назначают в дозе от 20 до 80 мг/сут однократно с вечерним приемом пищи или в 2 приема (утром и вечером). В последнем случае эффективность лечения несколько повышается. Начальную дозу 20 мг увеличивают на 20 мг через каждые 4 нед, если не достигнут желаемый уровень общего ХС плазмы крови. Доза мевакора должна быть уменьшена при снижении общего ХС ниже 140 мг%. Поддерживающее лечение мевакором должно проводиться в течение всей жизни.
Противопоказанием к назначению мевакора являются активные гепатит и цирроз печени, гипертрансаминаземия, индивидуальная непереносимость препарата, беременность и кормление грудью.
Взаимодействие с другими препаратами:. Имеются данные об увеличении протромбинового времени и риска кровотечений у больных, принимающих антикоагулянты непрямого действия на фоне лечения мевакором. В таких случаях рекомендуется более частый контроль показателей свертываемости крови.

Среди побочных действий, общая частота которых не превышает 1-2%, чаще всего встречаются метеоризм, диарея, запор, тошнота, боль в животе, сухость во рту, расстройства вкуса. Более редко (у 0,1% больных) наблюдаются кожная сыпь, зуд, головокружение, бессонница. При лечении мевакором, чаще в начальном периоде, возможно повышение уровня активности аланиновой и аспарагиновой трансаминаз в сыворотке крови. Если эти показатели не более чем в 3 раза превышают верхнюю границу нормы и не сопровождаются появлением каких-либо клинических симптомов, отмены мевакора не требуется. Редко повышается уровень щелочной фосфатазы, билирубина и креатинфосфокиназы. Последнее может сопровождаться симптомами миопатии (диффузные миалгии, размягчение мышц, многократное увеличение уровня креатинфосфокиназы), что требует отмены препарата. Большинство случаев миопатии наблюдалось у больных, получавших циклоспорин после трансплантации органов или такие гиполипидемические препараты, как гемфиброзил или никотиновая кислота. Частота миопатии на фоне монотерапии мевакором не превышет 0,1%. Лечение мевакором рекомендуется временно прекращать у любого больного при острых инфекциях, обширных хирургических вмешательствах, травмах, тяжелых метаболических нарушениях.
Для обеспечения безопасности лечения необходим биохимический контроль до назначения мевакора, а также ежемесячно в период подбора дозы (первые 2-3 мес лечения). В последующий период поддерживающей терапии биохимические анализы можно выполнять 1 раз в квартал. Более тщательный контроль необходим у больных, употребляющих значительное количество алкоголя. Все побочные эффекты проходят при уменьшении дозы или отмене препарата.
Правастатин (правахол) по механизму действия близок к ловастатину. Всасывается на 34%, биодоступность из-за эффекта “первого прохождения” через печень низкая – 18%. В крови на 50% связан с белками. Правастатин применяют в качестве активной формы; его метаболиты, образующиеся в печени, либо неактивны, либо обладают слабой фармакологической активностью. Т1/2 составляет 1,3-2,7 ч, максимальная концентрация в крови достигается через 1 ч. Элиминируется из организма путем билиарной секреции соединениями, которые не всасываются в кишечнике (до 70%), и с мочой (до 20%).
По данным 3-летнего исследования, применение правастатина у больных с ИБС и атеросклеротическим поражением сонных артерий привело к уменьшению скорости развития атеросклероза, а у части больных к регрессии бляшек в сонных артериях.
Побочные эффекты такие же, как у препаратов этой группы.
Симвастатин (зокор) представляет собой гипохолестеринемический препарат, получаемый синтетическим путем из продукта ферментации Aspergillus terreus. Является неактивным лактоном. После приема внутрь подвергается гидролизу с образованием бета-гидроксикислотного производного, которое представляет собой основной метаболит, оказывающий ингибирующее воздействие на З-гидрокси-3-метилглютарилкоэнзим А(ГМГ-КоА)-редуктазу – фермент, катализирующий начальную стадию биосинтеза холестерина, реакцию образования мевалоната из ГМГ-КоА. В связи с тем, что конверсия ГМГ-КоА в мевалонат представляет собой ранний этап биосинтеза холестерина, считается, что применение симвастатина не должно вызывать накопления в организме потенциально токсичных стеролов. Кроме того, ГМГ-КоА так же легко метаболизируется до ацетил-КоА, который участвует во многих процессах биосинтеза в организме.
В экспериментальных исследованиях на животных после введения препарата внутрь симвастатин с высокой избирательностью накапливался в печени, где его концентрация существенно превышала концентрации в других тканях.
Симвастатин быстро экстрагируется из крови при “первом прохождении” через печень (основное место его действия) и затем выводится с желчью. Концентрация активной формы симвастатина в системной циркуляции человека составляет менее 5% от принятой внутрь дозы; 95% от этого количества находятся в связанном с белками состоянии.
В многочисленных плацебоконтролируемых исследованиях было показано, что терапия симвастатином приводит к снижению уровня ХС на 20-30%, ХС ЛПНП – на 20-45%, аполипопротеина В – на 25-30%. Отмечено также более умеренное снижение уровня ХС ЛПОНП и повышение уровня ХС ЛПВП.
В нескольких контролируемых исследованиях было показано, что терапия дислипидемии может замедлить прогрессирование коронарного атеросклероза, хотя число больных, у которых отмечался регресс атеросклеротических изменений, был небольшим. Влияние симвастатина на течение атеросклероза было изучено в многоцентровом исследовании MAAS у 381 больного ишемической болезнью сердца. Симвастатин применяли в дозе 20 мг один раз в день вечером после еды. Больные контрольной группы получали плацебо. Длительность терапии составляла 4 года. Через 2 и 4 года больным проводили коронарографию и рассчитывали степень стеноза коронарных артерий. Критериями включения в исследование служили наличие атеросклеротических изменений по крайней мере в двух сегментах коронарных артерий (но без полной окклюзии), а также повышение уровня ХС сыворотки крови до 5,5-8 ммоль/л при уровне триглицеридов менее 4 ммоль/л. В результате лечения симвастатином отмечено снижение уровня ХС на 23%, ХС ЛПНП – на 31%, аполипопротеина В – на 28% и повышение уровня ХС ЛПВП на 9%. В контрольной группе была увеличена степень стеноза коронарных артерий в среднем на 3,6%, в то время как в основной группе она достоверно уменьшилась на 2,6%. При лечении зокором прогрессирование коронарных поражений наблюдалось реже (23 против 32%), а регресс – чаще (19 против 12), чем при приеме плацебо. Кроме того, у больных контрольной группы чаще отмечали новые поражения и полную окклюзию коронарных артерий. Клиническое течение в двух группах существенно не различалось, однако больным, получавшим симвастатин, реже требовалось проведение ангиопластики коронарных артерий или аортокоронарного шунтирования.
Целью другого исследования (скандинавское исследование выживаемости при применении симвастатина – 4S) было изучение влияния зокора на выживаемость 4444 больных (в возрасте 35-70 лет) со стенокардией и (или) инфарктом миокарда, у которых уровень ХС на фоне гиполипидемической диеты оставался повышенным до 5,5-8 ммоль/л (212-309 мг/дл).
Исследование проводили двойным слепым методом. Зокор назначали в дозе 20 мг/сут, при отсутствии достаточного эффекта дозу увеличивали до 40 мг/сут. Длительность терапии составляла в среднем 5,4 года (от 4,9 до 6,3 года). В результате лечения уровень ХС снизился в среднем на 25%, ХС ЛПНП – на 35%, а уровень ХС ЛПВП повысился на 8%. Наиболее важным результатом исследования 4S стало высокодостоверное снижение общей смертности (на 30%) и коронарной смертности (42%) под влиянием зокора. Смертность от других причин, помимо сердечно-сосудистых заболеваний, при применении зокора и плацебо не различалась. Лечение зокором привело также к снижению на 32% частоты развития различных осложнений ИБС (нефатальный инфаркт миокарда, остановка сердца с последующей успешной реанимацией). Больным, получавшим зокор, значительно реже (на 37%) требовалось проведение аортокоронарного шунтирования или ангиопластики коронарных артерий.
Экономический эффект от лечения определялся также снижением частоты госпитализаций по поводу ИБС у больных основной группы по сравнению с контролем.
Переносимость зокора при длительном применении была очень хорошей. Частота прекращения лечения из-за побочных эффектов (а они не отличались по характеру от других статинов) была одинаковой (6%) в группах больных, получавших симвастатин и плацебо. Рабдомиолиз, который считают наиболее опасным побочным эффектом статинов, наблюдался только в одном случае. После отмены симвастатина признаки рабдомиолиза быстро уменьшались.
Таким образом, в проведенном исследовании была впервые показана возможность реального улучшения прогноза у больных ИБС под влиянием холестеринснижающей терапии. Благоприятный эффект лечения отмечен не только у мужчин среднего возраста, но и у женщин и пожилых людей (старше 60 лет). Полученные исследователями данные позволяют рекомендовать применение зокора у всех больных, страдающих стенокардией и (или) перенесших инфаркт миокарда, у которых уровень ХС в крови превышает 5 ммоль/л, несмотря на соблюдение гиполипидемической диеты.
Флувастатин (лескол) является первым полусинтетическим ингибитором ГМГ-КоА-редуктазы: структурно близок к грибковым метаболитам и их аналогам.
При приеме внутрь быстро всасывается. Т1/2 составляет 30 мин. Интенсивно метаболизируется при эффекте “первого прохождения” через печень с образованием активных метаболитов, которые не проникают через гематоэнцефалический барьер. Низкая системная экспозиция определяет незначительное по сравнению с другими статинами число побочных эффектов (миозитов, расстройств ЦНС), связанных с фармакокинетическим взаимодействием. Фармакокинетика при сочетанном применении с ниацином, холестирамином, пропранололом, дигоксином не меняется. Обильная пища снижает биодоступность флувастатина. У больных циррозом печени снижается тотальный клиренс и увеличивается концентрация препарата в крови, хотя Т1/2 не меняется.
Принимают по 20-40 мг/сут. Многонедельное применение препарата снижает уровень ХС ЛПНП на 22,2% при дозе 20 мг/ сут и на 25,6% при дозе 40 мг/сут.
Эквивалентные дозы ингибиторов ГМГ-КоА-редуктазы приводят примерно к равному снижению уровня холестерина крови.
ПРОИЗВОДНЫЕ ФИБРОЕВОЙ КИСЛОТЫ. К этой группе относят клофибрат, безафибрат, гемфиброзил, ципрофибрат и фенофибрат. Общим в механизме гиполипидемического действия этих препаратов является повышение активности липопротеинлипазы, секреции желчи печенью и снижение продукции печенью триглицеридов. Степень влияния каждого из этих препаратов на уровень липидов крови зависит от типа гиперлипидемии и особенностей препарата. Чаще при лечении фибратами снижение уровня триглицеридов сопровождается повышением уровня антиатерогенного холестерина ЛПВП.
Клофибрат был первым препаратом этой группы, однако из-за побочных эффектов его применение ограничено.
Фенофибрат. Положительной особенностью фенофибрата по сравнению с другими фибратами является вызываемое им снижение уровня мочевой кислоты на 10-28%, что позволяет отдавать предпочтение фенофибрату при лечении больных с сочетанием гиперлипидемии и гиперурикемии. Кроме того, этот препарат наряду с ципрофибратом наиболее эффективно снижает уровень холестерина липопротеидов низкой плотности. Он используется при всех типах гиперлипидемии, за исключением I типа. Суточная доза в среднем составляет 200- 400 мг. Имеется пролонгированная форма препарата, принимаемая однократно в сутки. При гиперлипидемии Па типа достигается снижение уровня общего холестерина на 20-25%, холестерина ЛПНП – на 15-30%, триглицеридов при гиперлипидемии IIб и IV типов – на 40-60%, а степень возрастания уровня антиатерогенного ХС ЛПВП – до 22%. Положительное влияние фенофибрат оказывает также на аполипопротеины, повышая уровень апо- AI и апо-АII и снижая уровень апо-В и апо-Е.
Побочные эффекты наблюдаются у 2-15% больных: желудочно-кишечные расстройства (запоры или диарея), редко кожные проявления (зуд, покраснение, сыпь), быстро проходящие после отмены препарата. В единичных случаях отмечаются миалгия, сопровождающаяся повышением уровня креатинфосфокиназы, импотенция, общая слабость, головная боль, головокружение, бессонница. Иногда повышается уровень трансаминаз крови, в то время как уровни гамма-глутамилтранспептидазы и щелочной фосфатазы часто снижаются; эти изменения не сопровождаются клинической динамикой или изменениями в состоянии пациентов. Часто отмечается повышение литогенности желчи по сравнению с уровнем до лечения фенофибратом, однако до настоящего времени нет данных, свидетельствующих об увеличении частоты образования желчных камней на фоне лечения фенофибратом.
Безафибрат используется по тем же показаниям, что фенофибрат. Рекомендуемая суточная доза – 200 мг 3 раза в день, а при приеме пролонгированной формы эквивалентная доза составляет 400 мг/сут однократно. У пациентов с любым типом гиперлипопротеинемии безафибрат эффективно повышает уровень холестерина ЛПВП. Этот эффект препарата отмечается как у больных с первичной гиперлипидемией, так и с вторичной, обусловленной сахарным диабетом или заболеванием почек. При длительном применении безафибрата (от 2 до 4 лет) не отмечено развития толерантности к нему, эффект оставался стабильным. Гиполипидемическая эффективность безафибрата не уступает таковой клофибрата, фенофибрата, а степень повышения уровня холестерина ЛПВП выше. При сравнении безафибрата с ингибиторами ГМГ-КоА-редуктазы симвастатином и ловастатином установлено, что он более значительно повышает уровень холестерина ЛПВП; снижает уровень триглицеридов и холестерина липопротеидов очень низкой плотности (ЛПОНП), в то время как симвастатин и ловастатин эффективнее для снижения общего холестерина и холестерина ЛПНП. Частота побочных действий и их выраженность при лечении безафибратом не больше, чем при лечении другими фибратами. В основном это желудочно-кишечные расстройства и реже реакции – кожные и со стороны центральной нервной системы. Случаев гепатотоксичности за период клинического использования препарата не зарегистрировано, доказательств возрастания частоты образования желчных камней у пациентов, длительно принимающих безафибрат, нет.
Гемфиброзил хорошо всасывается в ЖКТ, максимум концентрации наблюдается через 1-2 ч. Т1/2 равен 1,3 ч, концентрация препарата в крови прямо пропорциональна дозе, однако при длительном применении препарат не накапливается. Метаболизируется путем окисления с образованием гидрокси- и карбоксиметиловых соединений. Конъюгированные с глюкуронидом метаболиты выделяются с мочой и лишь 6% – с фекалиями.
Результаты хельсинкского исследования, во время которого на протяжении 5 лет больных гиперлипидемией IIа, IIб или IV типа лечили гемфиброзилом в суточной дозе 1200 мг, продемонстрировали высокодостоверное – на 34% – снижение числа сердечно-сосудистых катастроф по сравнению с группой обследуемых, принимавших плацебо. В отличие от клофибрата достоверных различий в обшей смертности и частоте возникновения злокачественных опухолей между двумя группами пациентов не выявлено. Так же в отличие от клофибрата гемфиброзил не обладает сильно выраженной способностью к стимулированию образования желчных камней, хотя и вызывает увеличение литогенности желчи. При всех типах гиперлипидемий (за исключением I типа) гемфиброзил в дозе 800-1600 мг/сут особенно эффективен для снижения уровня триглицеридов – на 40-60%. Снижение общего холестерина и ХС ЛПНП достигает соответственно 20 и 23%. Уровень холестерина ЛПВП возрастает на 15-20%.
Среди побочных действий только желудочно-кишечные расстройства и сыпь наблюдались чаще при приеме гемфиброзила по сравнению с плацебо. Случаев гепатотоксичности препарата при клиническом применении не описано.

Ципрофибрат назначают по 100-200 мг/сут однократно. Его гиполипидемическая эффективность сопоставима с таковой у других фибратов. В некоторых исследованиях был показан регресс кожных ксантом у больных, лечившихся ципрофибратом. Убедительных данных о безопасности длительного применения ципрофибрата пока нет.
Свойство фибратов повышать активность липопротеинлипазы, снижать концентрацию триглицеридов плазмы, увеличивать уровень холестерина ЛПВП и усиливать действие гипогликемических препаратов делает их препаратами выбора при лечении больных сахарным диабетом, когда, несмотря на коррекцию гипергликемии, наблюдается гиперлипидемия.
ПРЕПАРАТЫ НИКОТИНОВОЙ КИСЛОТЫ. Никотиновая кислота снижает содержание и холестерина, и особенно триглицеридов. Суточная доза никотиновой кислоты, равная 3 г, обеспечивает падение уровня холестерина на 10%, а триглицеридов – на 28%. Эти изменения обусловлены уменьшением скорости синтеза ЛПОНП и не сопровождаются интенсификацией превращения ЛПОНП в ЛПНП, обнаруживаемой у пациентов с IV типом гиперлипопротеинемии при приеме фибратов. Скорость синтеза ЛПОНП снижется из-за уменьшения количества свободных жирных кислот, поступающих из жировой ткани, что отражает антилиполитическое действие лекарства. В результате падает уровень холестерина ЛПНП. Другим аспектом действия никотиновой кислоты является ее способность повышать уровень холестерина ЛПВП. Изучение метаболизма апо-АI указывает на то, что наблюдаемое изменение есть не что иное, как следствие индуцированного лекарством уменьшения скорости разрушения ЛПВП.
Побочное действие. Самым серьезным является расширение сосудов кожи. Это осложнение наиболее сильно выражено во время первых недель лечения. Позже, как правило, развивается толерантность к препарату (хотя и неполная), особенно если дозировку увеличивают постепенно: первоначально назначают по 0,25 г 1-3 раза в день и со временем переходят к максимальной дозе – по 1 г трижды в день. Эффект покраснения кожи можно уменьшить с помощью ацетилсалициловой кислоты, назначаемой перед никотиновой кислотой, которую следует принимать во время или после еды. Горячие напитки могут усилить эритему кожи. К другим побочным эффектам никотиновой кислоты относятся кожная сыпь, желудочно-кишечные расстройства, гиперурикемия, гипергликемия и дисфункция печени. В рамках Программы по исследованию коронароактивных средств установлено также учащение возникновения аритмий вследствие лечения препаратами никотиновой кислоты.
Хотя и существуют проблемы, связанные с применением эффективных доз никотиновой кислоты, большой опыт первичной и вторичной профилактики свидетельствует о том, что длительное использование этого лекарства как самого по себе, так и в сочетании с фибратами приводит к уменьшению смертности – общей и от сердечной недостаточности. Кроме того, никотиновая кислота усиливает лечебное действие неомицина, направленное на снижение уровня ЛП, и компенсирует нежелательный эффект этого препарата, состоящий в уменьшении концентрации холестерина ЛПВП. Никотинамид неэффективен как препарат, снижающий уровень липидов (цит. по Г. Томпсон).
Применяют также различные препараты на основе никотиновой кислоты, например никофуранозу и аципимокс.
Аципимокс – это 5-метил-4-окси-пиразинкарбоновая кислота. Было показано, что доза 750-1200 мг в день этого лекарства приводит к снижению уровня сывороточных триглицеридов и повышению содержания холестерина ЛПВП у пациентов с IV и V типами гиперлипопротеинемии. В отличие от фибратов аципимокс не вызывает увеличения постгепариновой липолитической активности, а активность печеночной липазы в его присутствии уменьшается; этим можно объяснить наблюдаемое возрастание уровня ЛПВП. Препарат не связывается белками, имеет время полужизни 2 ч и выводится почками в неизменном виде.
Эндурацин – новая лекарственная форма никотиновой кислоты с использованием особого вида тропического воска в виде матрицы. При приеме таблеток никотиновая кислота всасывается в кровь из кишечника равномерно медленно, что уменьшает число случаев отказа от лечения в связи с возникновением серьезных побочных реакций.
Есть основания полагать, что разница в действии нативной (кристаллической) никотиновой кислоты и эндурацина состоит лишь в частоте побочных действий; гиполипидемический эффект обоих видов никотиновой кислоты одинаков, хотя какие-то несущественные различия имеются. Лечение эндурацином лиц с гиперхолестеринемией приводит к значительному снижению уровня холестерина.
Наблюдается зависимость лечебного эффекта от дозы. Наибольшее снижение уровня общего холестерина (17%) наблюдается при назначении больших доз препарата (2 г/сут). Однако более выраженным оказалось влияние эндурацина на холестерин липопротеидов низкой плотности, уровень которого снижается на 38%. Следовательно, гиполипидемический эффект эндурацина в основном направлен на ЛПНП.
Другой особенностью действия эндурацина является его достаточно значимое влияние на уровень холестерина липопротеидов высокой плотности (ЛПВП). При этом не наблюдалось зависимости эффекта от дозы. Максимальное повышение (на 11%) отмечено при применении 1500 мг/сут. Частота побочных эффектов от приема эндурацина мало отличается от таковых при приеме обычной никотиновой кислоты.
Наблюдалось также некоторое повышение ферментов – аспарагиновой трансаминазы, лактатдегидрогеназы, щелочной фосфатазы, но это увеличение было в пределах допустимого.
АНИОНООБМЕННЫЕ СМОЛЫ. Анионообменные смолы, используемые для лечения гиперхолестеринемии, представляют собой нерастворимые соединения. Механизм действия заключается в связывании желчных кислот в просвете кишечника, что препятствует их реабсорбции и усиливает их фекальную экскрецию. В результате заметно активируется синтез желчных кислот, а следовательно, увеличиваются потребности клеток печени в холестерине. Это приводит к возрастанию количества поверхностных рецепторов ЛПНП, повышению скорости удаления ЛПНП из плазмы и в конечном итоге к уменьшению уровня холестерина ЛПНП, что и делает эти лекарства особенно полезными при лечении гетерозиготной формы СГХС, когда высокий уровень ЛПНП обусловлен лишь частичным нарушением рецепторопосредованного катаболизма ЛПНП. Однако использование препаратов ограничивается их неприятными вкусовыми качествами.
В случае гомозиготной формы СГХС анионообменные смолы неэффективны.
Холестирамин – полимер, содержащий аммониевые группы. В просвете кишечника обменивает ионы хлора на ионы желчной кислоты. Препарат выпускают в виде порошка, который перед употреблением размешивают в жидкости. Холестирамин принимают по 8-24 г в день, обычно разделяя это количество на 2-3 приема, но многие пациенты находят довольно затруднительным проглотить более двух порций (одна порция весом 9 г содержит 4 г смолы) дважды в день из-за побочных эффектов лекарства, связанных с желудочно-кишечными расстройствами. У больных с умеренной гиперлипидемией IIа и IIб типа средний уровень общего холестерина снижается на 8,5%, холестерина ЛПНП – на 12,6%, содержание холестерина ЛПВП возрастает на 3%, а триглицеридов – на 4,5%.
Среди побочных эффектов наиболее часто встречается запор, который иногда осложняется непроходимостью кишечника, а также диспепсией. Поскольку холестирамин затрудняет всасывание железа и фолиевой кислоты, оба эти вещества необходимо давать детям, принимающим препарат. Нарушение всасывания дигоксина и тироксина также может создавать определенные проблемы. Чтобы избежать их, рекомендуется пить эти лекарства в промежутках между приемами холестирамина.
Колестипол, представляющий собой сополимер тетраэтиленпентамина и эпихлоргидрина, по механизму действия близок к холестирамину. Взрослым назначают обычно по 10 г (2 порции по 5 г) 2 раза в день. Не считая холестирамина, колестипол является, по-видимому, единственным безопасным лекарством для детей, страдающих гиперхолестеринемией. По способности снижать уровень холестерина ЛПНП холестирамин и колестипол практически не различаются. Одинаковы и их побочные эффекты – увеличение гипертриглицеридемии при многолетнем приеме и желудочно-кишечные расстройства. Однако некоторые пациенты переносят колестипол лучше, чем холестирамин.

Неомицин – плохо всасываемый антибиотик. Эффективно снижает уровень холестерина при дозе 0,5-1 г 2 раза в день. Длительное применение антибиотика приводит к уменьшению у пациентов с СГХС концентрации сывороточного холестерина почти на 30%. Это эквивалентно терапевтическому воздействию холестирамина, принимаемого по 16 г в день. Неомицин препятствует всасыванию холестерина за счет образования с ним нерастворимых комплексов в просвете кишечника, что происходит в результате взаимодействия катионных групп аминогликозида (неомицина) с анионными группами смешанных мицелл, внутри которых находится холестерин. Наблюдается снижение уровня холестерина ЛПНП и ЛПВП.
Побочные эффекты: тошнота, предотвращаемая приемом лекарства вместе с пищей, и диарея. При длительном применении препарат может проявить ототоксичность, но связанное с этим осложнение у людей со здоровыми почками встречается редко. Применение неомицина ограничено из-за возможности возникновения побочных эффектов при продолжительном использовании и часто появляющегося поноса.
Пробукол – 4,4-(изопропилидендитио)бис-2, 6-ди(-бутилфенол) – обладает умеренной активностью в снижении содержания холестерина и оказывает очень незначительное воздействие на уровень сывороточных триглицеридов. При дозе по 0,5 г 2 раза в день этот препарат уменьшает концентрацию сывороточного холестерина у пациентов с IIа и IIб типами гиперлипопротеинемии на 20%, в случае IV типа – на 12%, а при СГХС – примерно на 10%. Падение уровня сывороточного холестерина является следствием снижения содержания холестерина как ЛПНП, так и ЛПВП. Несмотря на нежелательное уменьшение концентрации холестерина ЛПВП, пробукол вызывает регрессию ксантом, причем этот эффект лучше всего проявляется у пациентов с наиболее заметным снижением уровня холестерина ЛПВП.
Похожие статьи
- Противосудорожные средства. Характеристика
- Антитромботические средства. Характеристика
- Антиаллергические средства. Характеристика
- Муколитические средства. Характеристика
- Нестероидные противовоспалительные средства. Характеристика
- Пенициллины. Характеристика лекарственных средств
- Аминогликозиды. Характеристика препаратов
- Антимикробные средства. Принципы терапии
- Снотворные средства
- ПРОТИВОВОСПАЛИТЕЛЬНЫЕ И БОЛЕУТОЛЯЮЩИЕ СРЕДСТВА

